미국식품의약국(FDA)이 신약 허가심사비용을 405만 달러(약 53억)으로 책정하면서 글로벌 진출을 목표로한 국내 제약바이오 기업들의 부담이 커질 것으로 보인다.
올해 10월부터 신약 허가심사비용은 25% 인상됐으나 오히려 바이오시밀러는 41.7% 인하돼 바이오시밀러 기업들의 부담은 줄게 됐다.
한국바이오협회 바이오경제연구센터가 8일 발간한 이슈 브리핑에 따르면 미국 FDA는 신약(전문의약품), 제네릭, 바이오시밀러, 의료기기제조기업으로부터 받는 2024년 회계연도 허가심사수수료(User free)를 확정해 발표했다. 2024년도 회계연도는 올해 10월부터 2024년 9월까지다.
FDA는 매년 인플레이션, 심사 신청건수, 제조시설 수 등을 감안해 이용자인 기업으로부터 받는 허가심사수수료를 책정하고 있다.
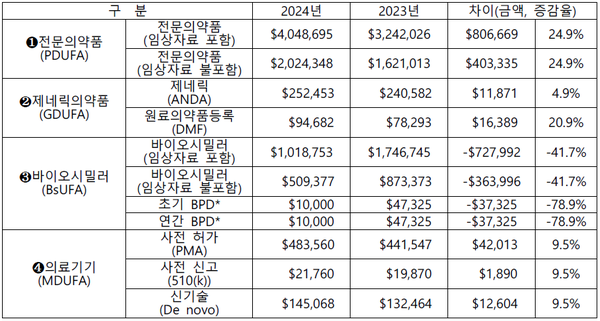
10월 1일부터 적용되는 전문의약품에 대한 2024년 허가심사 수수료는 사상 처음으로 4백만 달러를 돌파해 4,048,695달러(약 52억 9천 1백만 원)로 책정돼 지난해에 비해 24.9% 인상될 예정이다.
제네릭의약품과 의료기기도 인상됐다. 제네릭은 4.9% 상승돼 25만 2453만 달러(약 3억 3154만 원)으로 책정됐으며 의료기기는 9.5% 상승한 483,560 달러(약 6억 3476만 원)으로 인상됐다.
반면 바이오시밀러 허가심사 수수료는 41.7% 인하돼 1,018753 달러(약 13억 3721만 원)로 책정됐다.
전문의약품, 제네릭, 의료기기 모두 인상되는 가운데 바이오시밀러는 큰 폭으로 인하되는데 이는 2023년에서 이월된 약 2천만 달러(약 263억)의 바이오시밀러 운영비가 2024년 예산에 반영되면서 허가심사비용이 크게 낮아진 것으로 분석됐다.
바이오경제연구센터는 “2024년도 바이오시밀러 허가심사수수료 산정을 위한 시뮬레이션에서 임상자료가 포함된 14개의 바이오시밀러 허가심사 신청이 있을 것으로 예측된다”며 “새롭게 23개가 BPD(바이오시밀러제품개발)에 진입하고 97개가 연례 BPD에 적용되는 등 총 120개의 BPD가 예상돼 2024년에도 미국내 바이오시밀러에 대한 개발과 허가가 활발히 진행 될 것으로 전망된다”고 밝혔다.

